***Pour revenir à la page d’accueil** ICI
L’OSMOSE POUR LA PRODUCTION D’ENERGIE
Le sujet de
l’osmose est un peu comparable à celui de la mécanique quantique .
Les équations
fonctionnent parfaitement (quoique un peu moins bien dans le cas de l’osmose…)
Mais on est encore aujourd’hui à la recherche d’une explication qui serait au minimum intuitivement convaincante !!!
Une preuve en est le titre de cet article de 2012
« Five
popular misconceptions about Osmosis »
Alors que l’osmose était déjà mise en équation en 1887 par le chimiste néerlandais van’t Hoff !
Dans ce qui
suit, après une description du phénomène osmotique, puis des différentes
techniques mises en œuvre, nous
reviendrons sur ce débat en Annexe.
Description du phénomène
D'après Lydéric Bocquet , chercheur au CNRS.
"La différence entre les concentrations en ions de sodium (Na+) et de chlore (Cl-) dans l’eau salée et dans l’eau douce crée une énergie chimique appelée « énergie libre de Gibbs » lorsque les deux types d’eau se mélangent. Ce potentiel est lié à la deuxième loi de la thermodynamique et exprime l’entropie générée lors de ce processus. Par exemple, pour 2 m3 d’eau douce mélangée à 2 m3 d’eau de mer avec une concentration en sel de 30 g/L à 30 °C, cette énergie représente 1 kWh "
"
D’après
Wikipedia
« L'osmose est le phénomène de diffusion de la matière, caractérisé par le passage
de molécules de solvant d'une
solution vers une autre à travers la membrane semi-perméable qui sépare ces deux
solutions dont les concentrations en soluté sont
différentes ; le transfert global de solvant se fait alors de la solution
la moins concentrée (milieu hypotonique) vers
la solution la plus concentrée (milieu hypertonique)
jusqu'à l'équilibre (milieux isotoniques). Ce
phénomène concerne uniquement les échanges entre deux solutions liquides qui
ont des concentrations de solutés différentes,
séparées par une paroi semi-perméable.
Cette notion a permis de mieux comprendre le comportement des
solutions aqueuses en chimie, à la fin du xixe siècle ;
mais elle est aussi particulièrement utile en physiologie et
en biologie cellulaire pour expliquer les
échanges chimiques au sein des organismes vivants. »

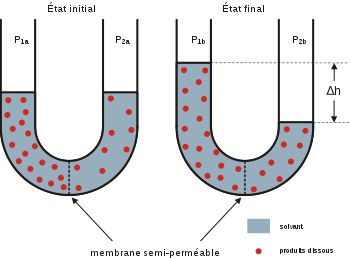
Pour simplifier, nous nous placerons dans le cas où seule la partie gauche contient du soluté (chlorure de sodium NaCl , eau de mer par exemple) et la partie droite de l’eau pure comme solvant.
La membrane semi-perméable bloque totalement les molécules de sel ( on verra plus tard
sa dissociation en ions) représentées en rouge.
Avec le
temps, on assiste donc à une montée du coté salé et bien entendu à une descente du côté de l’eau.
Si l’on
obture le tube à gauche, une « pression osmotique »se développe dont la
valeur est étonnamment forte, supérieure à 25 bar avec de l’eau de mer salée à 35
g/litre.
Cette
pression est directement proportionnelle la concentration en sel et à la température
absolue, exprimée en Kelvin.
On verra que
cette énergie chimique transformée en énergie mécanique et liée au mouvement
Brownien des molécules de soluté.
L’énergie
potentiellement récupérable est considérable.
Certains
projets-pilotes sont en cours, notamment
dans le delta du Rhône.
La pression
Calcul de la pression osmotique
La pression osmotique peut se calculer en assimilant les molécules de soluté dilué dans le solvant à un gaz parfait. Ceci est valable dans la mesure où la concentration en soluté reste relativement faible.
P
= i(n/V)RT
P bar
I facteur de dissociation 1, 2, 3 typiquement
V l (litres)
R constante des gaz parfaits 0.08206 l.bar/mol. K K température en Kelvins
n nombres de moles de soluté
Une mole comprend NA unités, avec NA = 6.02 10**23 le nombre d’Avogadro.
Pour calculer une masse molaire d'une molécule on utilise sa
formule chimique et la masse atomique de chaque élément
convertie en grammes. Son unité est la « mol ».
Par exemple 12 pour le carbone C, 1 pour l’hydrogène H, 16 pour l’oxygène O, 23 pour le sodium Na, 35.5 pour le chlore Cl.
Ces chiffres correspondent approximativement à la quantité de protons + neutrons de chaque atome.
L'existence d'isotopes (neutrons additionels) en proportions variables peut donner une valeur non entière: 35.5 pour le chlore.
EXEMPLE du sucrose
Dans le cas
du sucrose de formule
C12 H22 O11
C=12 donc
12x12 = 144
H=1 donc 22x1
= 22
O=16 donc
16x11 = 176
Une mole de
sucrose soit 6.02 10**23 molécules pèsera donc
144 + 22 + 176 = 342g = 1mol
Le sucrose
dissout reste sous forme d’une seule molécule, donc le facteur de dissociation
i = 1.
A la concentration de 1 mol/litre, soit 342g/litre d’eau, à la température de 25° C, soit 273+25 = 298 K, la pression osmotique du sucrose est
P= 1(1)x0.08206x298 = 24.4 bar
EXEMPLE de l’eau de mer
Une mole de
chlorure de sodium NaCl pèse 23 + 35.5 = 58.5g
L’eau de mer moyenne
est à 35 g/l, donc le nombre de moles par litre est de
35/58.5 ~ 0.6
mol/l
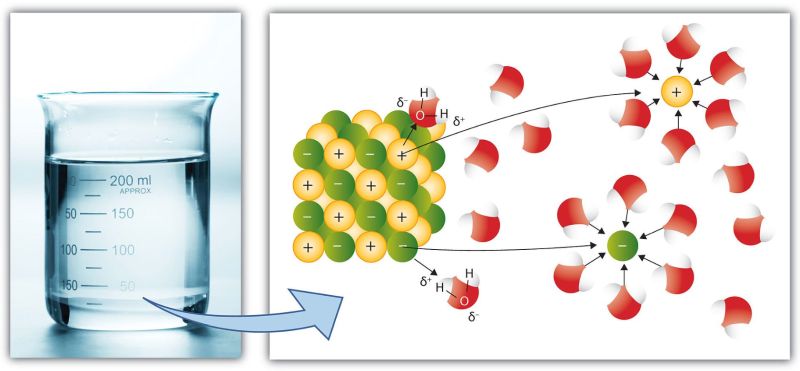
Contrairement au sucrose, le sel se dissocie dans l’eau en deux ions, Na+ et Cl-.
L'asymétrie des charges electriques
de la molécule d'eau avec ses deux atomes H+ et un atome O- crée
une attraction vers les ions Na+ et Cl- du sel dissout.
Dans la formule P = i(n/V)RT
L’expérience prouve que
1.8 est plus proche de la réalité : en cause l’appairage aléatoire
de certains ions qui réduit donc le nombre de particules.
P = 1.8 x0.6 x0.08206x298 = 26.4 bar
Dans la vraie
vie, c’est la membrane semi-perméable qui plafonne le rendement des procédés osmotique de
génération d’énergie : la taille très
réduite de ses pores limite considérablement le débit
.
C’est la
découverte des capacités de débit surprenantes des nanotubes de
carbone qui a relancé l’intérêt dans ces potentielles
sources d’énergie considérable.
Les différentes techniques de génération
--PRO
Pressure Retarded Osmosis
Cette
technique est la plus classique.
Un
sérieux problème est la limitation du
débit par l’utilisation de membranes classiques
--RED
Reverse Electro Dyalisis
--Membranes basées sur la nano fluidique
C'est le
chercheur Lydéric Bocquet (CNRS) qui est à l'origine de nombreuses découvertes dans le domaine.
« Au-delà de ces résultats en laboratoire, ce qui rend la nanofluidique unique, c’est le chemin court que ce domaine offre entre la science fondamentale et les applications. La nanofluidique est en train de révolutionner le domaine des membranes avec des matériaux et des concepts nouveaux pour le traitement des eaux polluées, le dessalement de l’eau de mer ou la production d’énergie. Les propriétés émergentes des fluides aux nanoéchelles, couplées aux plus récents nanomatériaux, sont autant d’atouts pour développer de nouvelles technologies. Ainsi, au vu du comportement unique du carbone comme canal fluidique, les matériaux à base de cet élément ont un rôle clé à jouer dans ce contexte. Par exemple, les membranes en graphène intègrent déjà des dispositifs de dessalement de l’eau. De même, les membranes dites « d’oxyde de graphène », qui sont des millefeuilles de flocons de graphène, réalisent une combinaison quasi idéale : elles sont faciles à fabriquer à grande échelle et combinent la nature 2D des feuilles de carbone, une perméabilité élevée et une excellente capacité de tamisage et de sélectivité due à l’espacement subnanométrique entre les flocons de graphène. »
" En 2006, Olgica Bakajin, du laboratoire américain Lawrence-Livermore, et ses collègues ont fait une découverte très intrigante : les écoulements de l’eau au travers de membranes constituées d’un assemblage de milliards de nanotubes de carbone de 2 nanomètres de diamètre étaient jusqu’à 10 000 fois plus forts et rapides que ce qui était anticipé sur la base des prédictions usuelles de l’hydrodynamique. Ce résultat inattendu a suscité un débat considérable dans la communauté. Fallait-il remettre en cause l’équation maîtresse de l’hydrodynamique (l’équation de Navier-Stokes) ? Ou bien était-ce la démonstration d’un nouveau phénomène, en l’occurrence un frottement anormalement faible de l’eau sur les parois des nanotubes ?"
"Avec cette théorie de frottement quantique, nous expliquons pour la première fois pourquoi l’eau frotte beaucoup dans les gros nanotubes multiparois, qui ressemblent à du graphite légèrement courbé, tandis que le frottement disparaît vite dans les nanotubes plus petits, où la courbure plus importante de la paroi conduit à un découplage des différentes couches et la disparition du mode plasmon.
Le
freinage quantique disparaît dans les petits tubes et les écoulements
deviennent ultrarapides ! Ces couplages quantiques, restés largement inaperçus
jusqu’ici, donnent enfin une explication aux résultats expérimentaux déroutants
sur le frottement dans les nanotubes de carbone."
Ces extraits
proviennent de l’article « Au-cœur des étonnants flots moléculaires »
publié dans Pour la Science
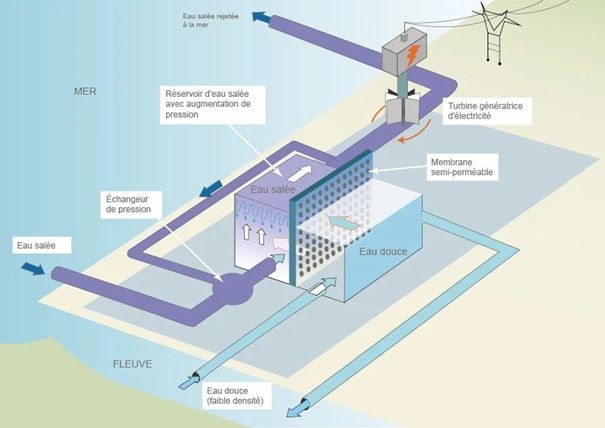
« La
Start-Up bretonne Sweetch Energy
s’est associée à la Compagnie Nationale du Rhône (CNR), premier producteur
français d’électricité 100 % renouvelable, pour lancer un projet ambitieux. Il
s’agit de construire la première usine pilote de production à grande échelle
d’électricité osmotique en France. Le site sera établi dans le delta du Rhône
d’ici 2023. C’est le premier partenariat industriel français dans ce secteur.
Le but d’une telle installation est d’utiliser le potentiel incroyable de ce que l’on nomme l’« énergie bleue ». D’après Sweetch Energy, la production mondiale que l’on peut attendre de cette énergie est de l’ordre de 27 000 TWh par an, ce qui correspond à la consommation d’électricité de toute l’humanité. »
Cette technologie baptisée INOD utilise ce
nouveau type de membrane nano fluidique.
ANNEXE
Cette
interprétation de l’origine de la pression osmotique provient de l’article ci joint en pdf.
« Five
popular misconceptions about Osmosis »
Après van’t Hoff (assimilation à un gaz parfait) , Gibbs en
1897 construisit la théorie thermodynamique correcte de l’osmose.
Basée sur
l’énergie libre et l’entropie, elle est rigoureuse, mais complexe et n’éclairant pas l’origine physique du phénomène.
Il n’est donc
pas surprenant qu’au cours du temps d’autres explications plus intuitives
furent développées en particulier visant le monde de la biologie,
particulièrement concerné par l’étude
des membranes cellulaires.
Hélas ces
théories, encore répandues de nos jours, sont démontrées fausses dans
l’article.
Les auteurs
en revanche proposent ce modèle :
Les
particules de solutés s’agitent selon les règles du mouvement Brownien :
chocs de valeur et de direction aléatoire, dépendant de la température (voir la vidéo et l'explication ci dessous)
Quand une particule heurte la membrane celle-ci est renvoyée dans une direction momentanément fixe:
la membrane oriente momentanément le mouvement Brownien et lui soutire de l'energie.
Durant ce
déplacement, la molécule de soluté entraine par interaction visqueuse des
molécules de solvant à proximité de la membrane .
Ceci
correspond à alors une action répulsive de la membrane sur l’ensemble soluté +
solvant situé à sa gauche.
Ce mouvement
de liquide crée un appel pour les molécules de solvant qui traversent la
membrane sans aucune résistance de la droite vers la gauche.
Ce flux à
sens unique explique l’augmentation du niveau à gauche, donc de la
pression hydrostatique.
compare cette action de la membrane qui « sélectionne » une direction dans un ensemble de valeur moyenne nulle, au rôle d’une diode « rectifieuse » en électronique.
Alimentée par un courant alternatif de valeur moyenne nulle, la diode ne laisse passer que la partie positive du signal, donc extrait/génère un signal moyen non nul.
********************Le mouvement Brownien*******************

**************************Références************************
https://www.chemteam.info/Solutions/Osmosis-Equation.html
https://www.chemteam.info/Solutions/Osmosis.html
https://www.academia.edu/26990894/Five_popular_misconceptions_about_osmosis
https://www.pourlascience.fr/sd/physique/au-coeur-des-etonnants-flots-moleculaires-24128.php
https://www.sweetch.energy/who-we-are
https://www.agence-france-electricite.fr/actualites/nouvelle-centrale-osmotique-rhone/
https://www.sciencedirect.com/topics/engineering/pressure-retarded-osmosis PRO
https://fr.science-questions.org/questions_de_science/166/Qu_est-ce_que_le_mouvement_brownien/#:~:text=L'%22amplitude%22%20du%20mouvement%20Brownien%20augmente%20donc%20avec%20la,les%20mol%C3%A9cules%20sont%20plus%20nombreuses.fr.science-questi
